APASL热点 | 七成亚裔慢乙肝患者有肾损害风险,抗病毒治疗不能只看疗效
- 分享
前言:
今年的亚太肝病学会年会(APASL2020)又在春光明媚时如约而至,但今年我国的肝病和感染病医生正不计生死地战斗在抗疫一线,无暇前往。为支持他们在战疫间隙的学术交流需求,亚太肝病学会中国大陆委员会联合中华医学会肝病学分会、中华医学会感染病学分会、中国肝炎防治基金会发起了免费公益网络直播活动,国际肝病作为承办方之一参与其中,与有荣焉!为广大肝病和感染病领域工作者传递APASL2020上的最新肝病进展,是我们以微薄力量参与抗疫的方式之一。
我国有2000万~3000万例慢性乙型肝炎(慢乙肝)患者[1],作为肝病医生,应当尽可能地为他们提供最安全和最有效的抗病毒治疗。在APASL2020上,一项针对亚裔慢乙肝患者骨肾功能风险改善的研究[2]或许能为我们进一步接近这个“最安全和最有效”提供参考。河北医科大学第三医院南月敏教授应邀拨冗解读该研究,帮助大家学习。
研究为随机、双盲、非劣效性的III期试验,纳入接受TDF治疗≥48周且HBV DNA低于检测下限≥12周,筛查时HBV DNA<20 IU/mL的患者。按1∶1随机分组,一组继续TDF治疗,一组换用TAF治疗,在48周时评估两组的抗病毒疗效以及肾脏、骨骼安全性。共招募了541例患者,最终488例纳入分析(TAF组243例,TDF组245例),为整体队列。这些患者中400例为亚裔(亚裔患者队列),72%(288例)有至少一种TDF危险因素。
TDF危险因素指:老年(>60岁),骨病(髋或脊柱T评分判断骨质疏松),肾损害(慢性肾病分期≥2,即基线估计肾小球滤过率<90 mL/min),白蛋白尿(UACR>30 m/g),低磷血症(血磷<2.5 mg/dL),肥胖(BMI≥30 kg/m2),共患病(心血管疾病,糖尿病,高脂血症或高血压)。
(1)抗病毒疗效
整体队列中,48周时,换用TAF治疗的疗效不劣于继续使用TDF治疗,HBV DNA ≥ 20 IU/mL的患者在两组均<1%(各有1例;比例相差0%)。在亚裔人群亚组中的结果相似,有TDF危险因素者换用TAF组和继续使用TDF组的病毒学应答率分别为96.5%和96.6%,无TDF危险因素的两组则分别为98.1%和95.0%。
(2)肾脏安全
全体队列和亚裔有TDF危险因素亚组队列的结果一致:换用TAF治疗组患者的估计肾小球滤过率(eGFRCG)增加(表1),亚裔有TDF危险因素人群亚组中换用TAF治疗者的eGFRCG增加2.6(中位数),而继续使用TDF组下降2.7(中位数),P<0.0001;近端肾小管功能受损标志物水平下降(图1,图2)。
表1. 48周时估计肾小球滤过率(eGFRCG)相对于基线的变化(mL/min)
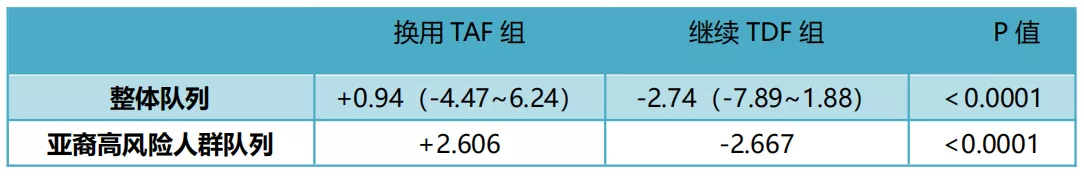
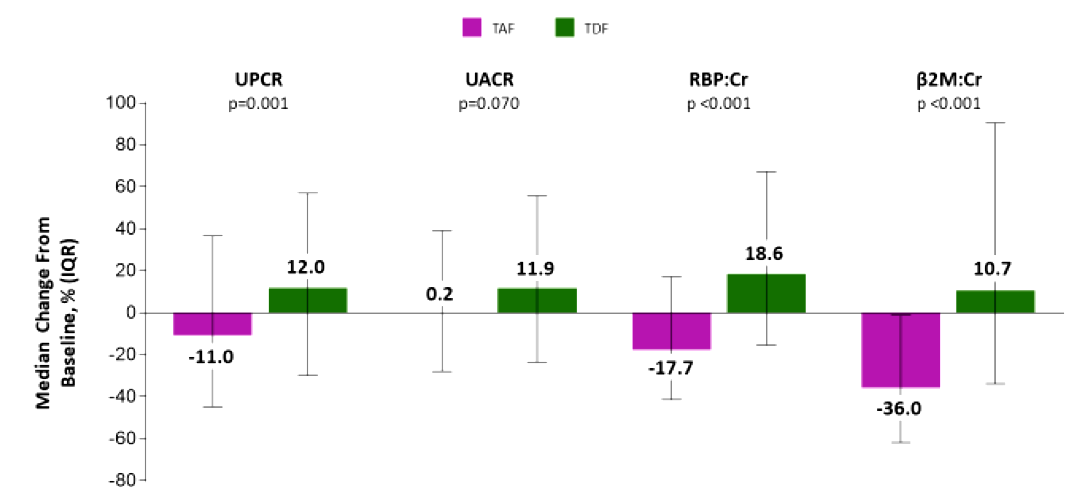
图1. 整体队列基线和48周蛋白尿定量标志物的变化
(β2M,β2微球蛋白;RBP,视黄醇结合蛋白;UACR尿白蛋白/Cr比值;UPCR,尿蛋白/Cr比值)
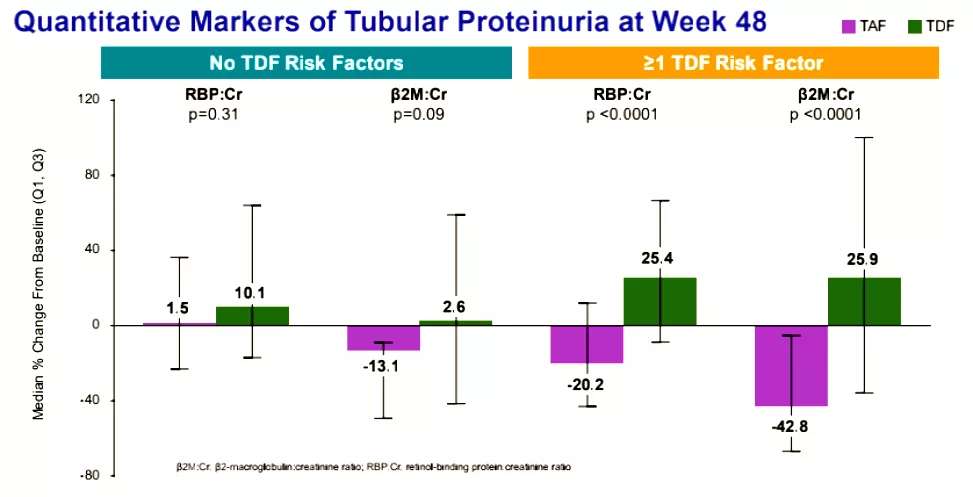
图2. 亚裔人群亚组基线和48周肾小管蛋白尿定量标志物的变化
(3)骨骼安全
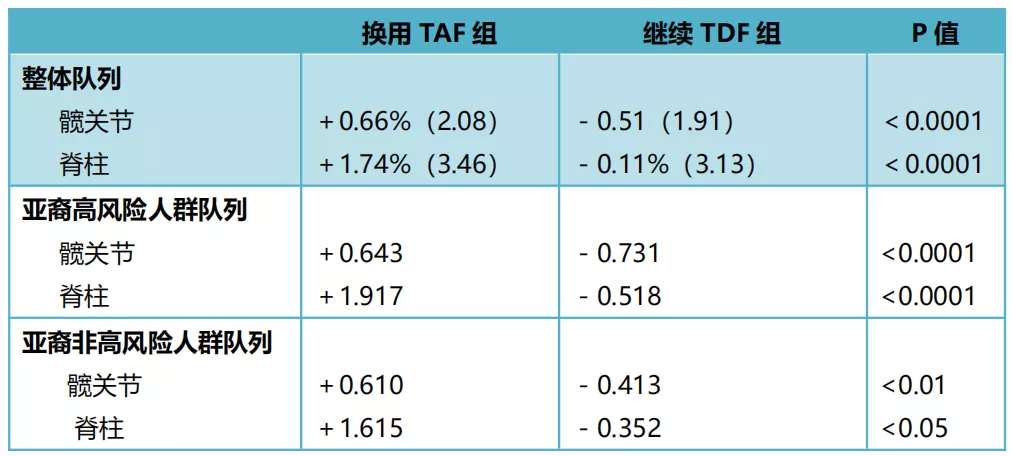
整体队列和亚裔人群亚组队列的结果一致:换用TAF治疗组患者的髋和脊柱的BMD增加(表2),骨周转标志物受影响的程度更轻;而继续使用TDF组的骨密度下降。
表2. 48周时髋和脊柱的骨密度相对于基线的变化(%)
(4)生化学应答和血清学应答
整体队列中,换用TAF组ALT正常的患者比例在数值上高于继续使用TDF组(图3),ALT复常率高于继续使用TDF组(按AASLD2018标准有统计学意义,P=0.014)。两组的血清学应答情况相似。
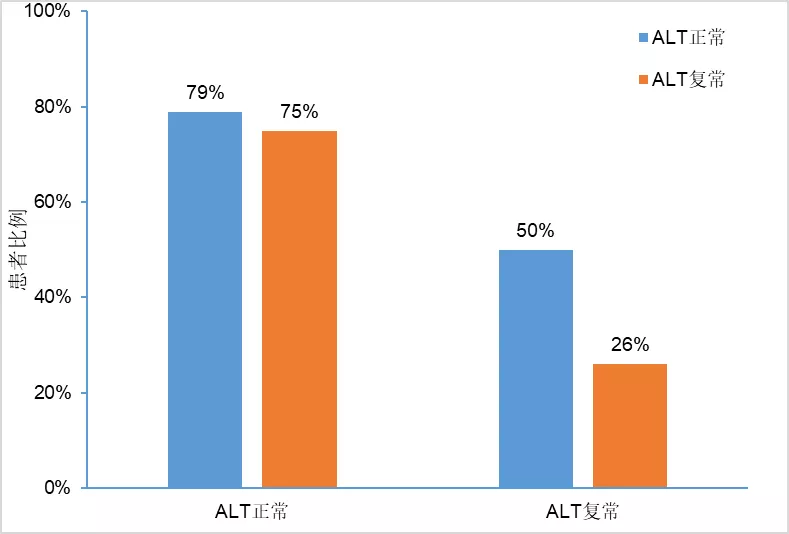
图3. 换用TAF和继续TDF治疗48周的生化学应答
图中数据来自整体队列,使用AASLD2018标准(35/25 U/L)。ALT正常率指48周时ALT水平正常的患者比例,无论基线时的ALT水平;ALT复常率指基线时ALT水平异常、48周时ALT水平正常的患者比例。
(5)对整体队列的分析未发现病毒耐药。
(6)整体队列和亚裔患者队列中,3-4级不良事件和严重不良事件的发生率低,两个治疗组间相似。
TAF治疗慢乙肝可改善安全性且不影响抗病毒疗效,可替代TDF。
亚裔慢乙肝患者中:有≥1个TDF危险因素人群亚组中,将TDF换成TAF治疗48周,可显著改善患者的骨骼和肾脏指标;在无TDF危险因素亚组中,换用TAF治疗同样显著改善骨骼指标,并且肾脏指标也有改善趋势;在所有患者中,换用TAF治疗维持高抗病毒疗效,与TDF治疗的患者相似。
南月敏教授解读:
这是首个在TDF治疗应答良好的乙肝患者中研究换药(换用TAF)效果及安全性的随机对照试验,为既往的研究的重要补充。APASL上报告的研究主要针对其中的亚裔、有肾损害高风险的患者。从研究结果中可以得到以下信息:
①使用TDF治疗已经取得病毒学抑制的慢乙肝患者换用TAF治疗,也可以取得同样的病毒学抑制,两种药物的抗病毒疗效是相似的。
②特别值得提出的是在安全性方面,TAF治疗组的肾功能指标,包括肾小球滤过率以及肾小管功能的一些指标都明显改善。而且TAF组的骨密度以及相关的骨磷代谢指标,包括骨形成、骨丢失这些骨周转标志物的水平也有明显改善,所以说TAF对骨骼的影响是一个良好的效果,也就是向好的方向转变。
③在此基础上,整体队列中TAF组的ALT复常率高于TDF组(按AASLD2018标准,P值为0.014;按中心实验室标准,差异无统计学意义)。同时两组的安全性和耐受性都很好,3级以上的不良事件发生率都很低。
各大学会慢乙肝管理指南[1,4,5]近年都更新了一线口服抗病毒药物的推荐,在原有的恩替卡韦和TDF基础上增加了TAF,国内外指南建议一致,希望大家在临床用药时充分考虑患者的状况,包括肝病本身和肝外重要脏器损害危险因素,特别是肾脏、骨骼危险因素的存在,来选择合适的药物。目前,亚洲慢乙肝患者人群中老龄化、存在危险因素的比例较高,在APASL2020上公布的这项研究中,400例亚裔患者中有一种以上TDF危险因素的比例达到了72%,其实在真实世界中这样的患者比例也比较高。TDF的“危险”,主要针对的是TDF对肾脏、骨骼代谢的影响。根据EASL2017慢乙肝指南[4],肾损害高危因素包括:失代偿肝硬化,肌酐清除率<60 mL/min,控制不佳的高血压、蛋白尿、未控制的糖尿病,活动性肾小球肾炎,同时应用肾毒性药物,或实体器官移植等。
对有这些危险因素的患者,我们应该更加关注他们肾脏和骨骼代谢的安全性。这项研究提示我们,对于这些存在危险因素的患者,在选择口服抗病毒药物时,TAF可能是一个良好的选择。同时,如果是在原有TDF治疗并获得良好病毒学应答的基础上,我们可以考虑直接换用TAF,能获得骨代谢以及肾脏安全性的改善。因为TAF是一个强效的抗病毒药物,可以直接换用,对未来的病毒学应答没有影响。(EASL对肾损害/肾损害高危人群的管理流程总结如图2。)
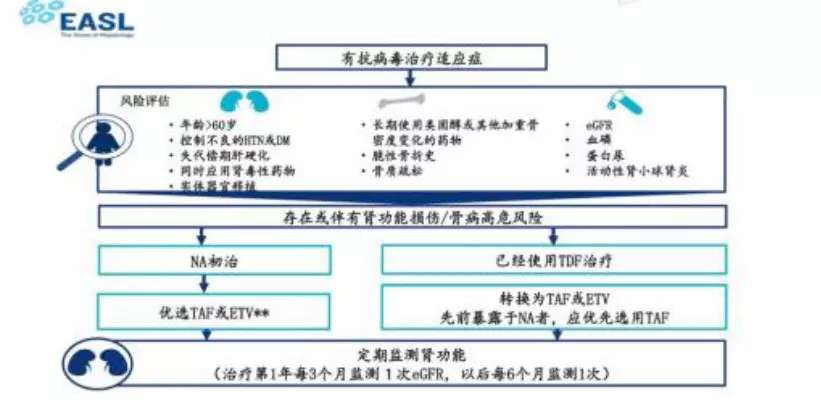
图2. EASL对肾损害/肾损害高危人群的管理流程
(**:eGFR<50 mL/min时,需调整ETV剂量)
另外,对于肌酐清除率<50 mL/min的患者,我国指南建议,如使用ETV和TDF,均需调整剂量,TAF在肌酐清除率<15 mL/min且未接受透析的患者中无推荐剂量,其余情况无需调整剂量。
南月敏教授最后表示:虽然TAF在我国上市应用的时间较短,但根据它和TDF相比的相似性和结构上的优势(使得TAF相对于TDF血浆半衰期长、稳定性高,靶向递送至肝细胞,全身暴露减少90%以上[6-9],图3),可能未来是一个比较受欢迎、能获得比较满意的病毒学应答又有较好安全性的药物。但我国肝病医生仍然需要加强临床观察,研究TAF在我国患者中的病毒学应答、生化学应答、治疗后肝病的长期预后和转归以及肝外的长期安全性,总结出我们的结果,来指导我国慢乙肝抗病毒治疗难治人群的用药选择。
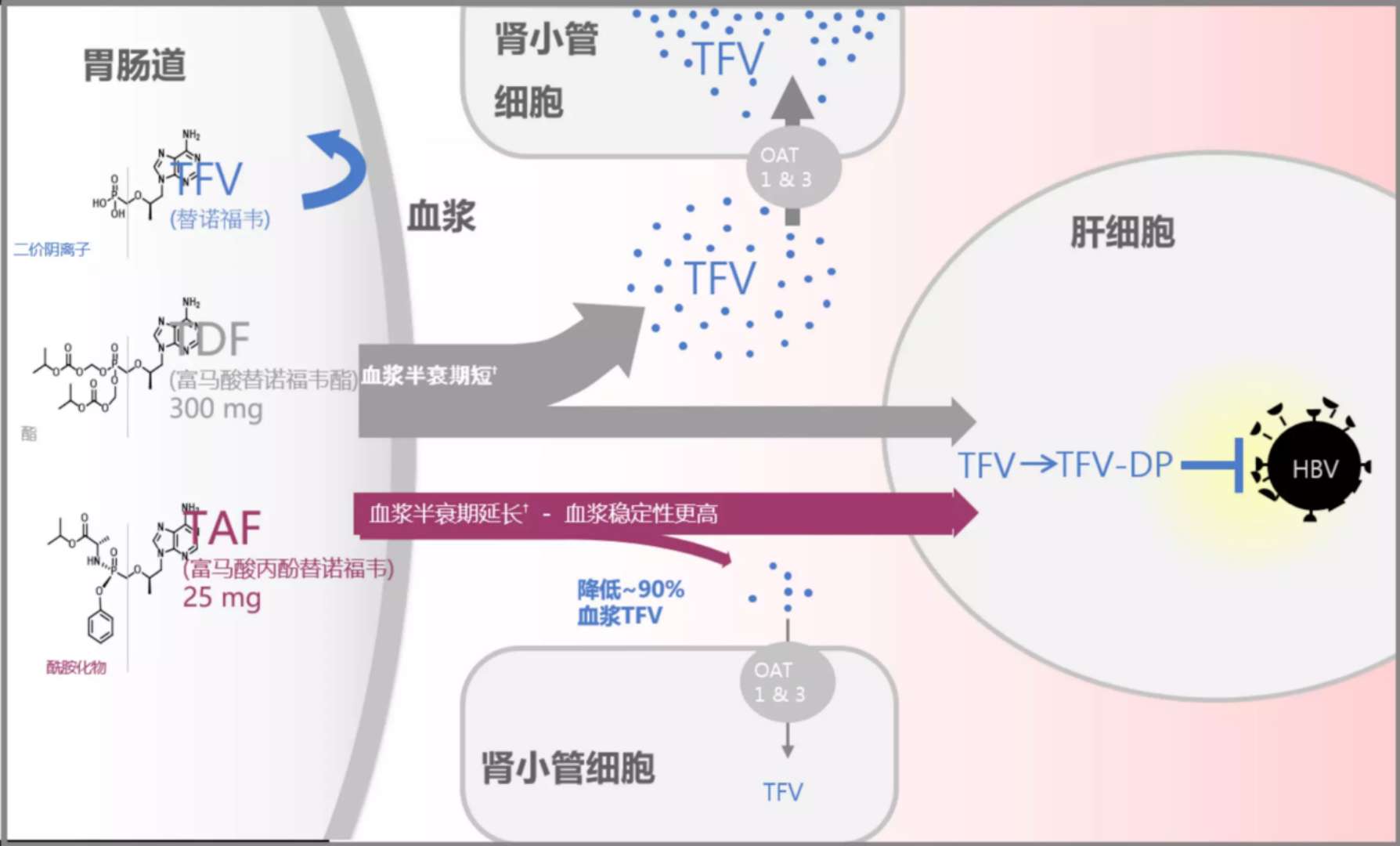
图3. TAF和TDF的药代动力学特点
(来源:《国际肝病》编辑部)

